Cristalografía/Conceptos básicos
Dado un determinado sistema cristalino, de él se puede deducir cierta información que repercute en las propiedades físicas macroscópicas. En particular, nos centraremos en los siguientes conceptos:
- Población de celda, es decir el número de átomos (iones, moléculas, etc.) contenidos en una célula.
- Coordinación de un átomo (ion, molécula, etc.), es decir, el número de sus vecinos más cercanos en el cristal
- Compactibilidad de un cristal, es decir, la relación entre el volumen de los átomos de una celda y el volumen de la celda.
- Densidad de un cristal, es decir, la relación entre la masa de una celda y su volumen.
Por cierto, Se tiene que redefinir el significado preciso a la compactibilidad de cristal.
Compactibilidad de un cristal
[editar]
Si partimos de que las partículas son esféricas la pregunta sería:
- ¿Cuál es la mejor manera de apilar esas esferas?
Aquí hay una solución simple:
- Si colocamos tres esferas para formar un triángulo equilátero
- Se coloca una cuarta esfera sobre el hueco formado por las anteriores
- Empezamos de nuevo hasta que el espacio esté pavimentado.
De hecho, hay dos formas de hacer una pila de este tipo:
Supongamos un plano pavimentado con esferas, denotado por A. Podemos, colocando esferas en los huecos, crear una nueva capa, denotada B. Se puede formar una tercera capa, ya sea colocando esferas sobre las esferas de A, hablamos de apilamiento ABA o colocando esferas desplazadas de las de A y B, hablamos de apilamiento ABC.
Tomando el modelo de “esferas duras”, una pila compacta se caracteriza por una compacidad máxima, igual a:
Respectivamente, hablamos de dos formas:
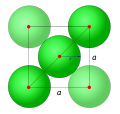
Pila cúbica centrada en las caras
[editar]La pila cúbica centrada en caras se caracteriza por los nodos de su red que se ubican:
- Los 8 vértices de un cubo
- En el centro de las caras de este cubo.
- La malla tiene 14 nodos, pero algunos de estos nodos se comparten con las mallas vecinas: los ocho vértices se comparten cada uno con ocho mallas, los 6 nodos en el centro de las caras se comparten entre dos mallas.
- El número de nodos específicos de la malla es así:
Más concretamente, esto significa que 4 átomos pertenecen propiamente a la celda (si solo consideramos lo que está dentro del cubo formado por la celda).
- Un ejemplo son los cristales de sal.
Pila hexagonal compacta
[editar]El otro conjunto compacto es la pila hexagonal compacta que se caracteriza por:
- La malla que estamos estudiando en este caso es un prisma derecho en forma de diamante (1/3 de la malla hexagonal) llamado "malla convencional".
- Cada mitad de la base del diamante se llama "triángulo equilátero".
- Esta malla se caracteriza por la presencia de: 8 nodos, coincidiendo con los vértices del prisma.
- Hay un nodo “central” ubicado a la mitad y debajo del centro de gravedad de uno de los triángulos equiláteros.
- La malla convencional tiene 9 nodos, de los cuales los primeros ocho se comparten con 8 mallas vecinas, por lo que cuenta con: nodos.
- El átomo central forma con el triángulo equilátero subyacente al tetraedro regular.
- Un ejemplo son los cristales de berilo
Radio Atómico
[editar]Las fuerzas de cohesión de las que estamos hablando son atractivas, al menos a media distancia. A corta distancia, los electrones de los átomos (o iones, o moléculas) se repelen entre sí, de ahí el modelo de "esferas duras", que define la noción de "radio atómico", que se analiza a continuación.
Podemos definir el "radio atómico", correspondiente al de las esferas del modelo, de diferentes formas. Cada uno está adaptado en ciertos casos:
- Radio atómico teórico - obtenido de la teoría de Slater, bastante inconveniente en cristalografía e incluso poco realista.
- Radio metálico: la mitad de la distancia entre los vecinos más cercanos del cristal metálico.
- Radio covalente: la mitad de la distancia entre los vecinos más cercanos del cristal covalente.
- Radio iónico: denotamos et los respectivos radios del catión y el anión, luego la distancia entre un catión vecino más cercano y un anión está .
Nota: En general, el radio del anión es mucho mayor que el del catión.