Curso de Química:Grupos funcionales
Los grupos funcionales en química orgánica son un conjunto de átomos que dan a la molécula (o a una parte de ella) unas propiedades concretas. Pasemos a ver los tipos:
Alcanos
[editar]Se trata de compuestos cuya composición incluye tansolo carbonos e hidrógenos todos ellos unidos por un enlace simple.
Esto corresponde a una fórmula general:
Estos se subdividen en cuatro grupos:
Lineales
[editar]Son aquellos que corresponden a una estructura del tipo:
Ramificados
Tienen una estructura similar a los lineales pero en estos en algun átomo de carbono de la cadena tiene en lugar de un hidrógeno otra cadena de tipo alcano. Dicho de una manera burda sería como "un alcano con alcanos enganchados"

Ciclicos
[editar]Estos son unos alcanos peculiares ya que no cumplen del todo la relación Esto se debe a que al ser cíclicos deben tener una unión carbono carbono en el lugar de una unión carbono-hidrógeno; lo que restaría un hidrógeno a cada uno de los átomos de carbono que se unen. Esto hace que respondan a una fórmula general del tipo:
Los alcanos cíclicos (obviamente) deben estar formados como mínimo por 3 átomos de carbono. Cabe hacer una apreciación dentro de estos ciclos. Los átomos de carbono, al ser alcanos tienen hibridación sp3, lo que hace que su ángulo de enlace más estable sea 109,3º. Sabiendo esto veamos unas imágenes:


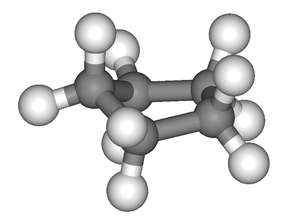

Cabe notar, que en el ciclohexano a pesar de que los sustituyentes tengan distinto color, representan todos a hidrógenos.
En estos se puede ver, que el ciclo de tres miembros y el de cuatro se alejan bastante de un ángulo de 109,3º. Esto hace que la molécula sea relativamente inestable y les ofrece unas propiedades bastante características. A parte de ello tambíen se nota que los cicloalcanos de 5 o más miembros se "retuercen" en si mismas para dar unas estructuras con ángulos de enlace más cercanos a 109,3º como es obvio, a medida que las moléculas tengan más átomos de carbono, se retorcerá más dando estructuras más plegadas. Los grupos funcionales contienen una base lo que se nombra como neurolitos que sirven para expandir la molecula y hacer una division notable.
Policíclicos
[editar]Se trata de moléculas, al igual que en el caso anterior en la que se rompen dos enlaces C-H para formar un enlace C-C, con la única diferencia de que en este caso dicho proceso ocurre dos veces, sobre tres o cuatro átomos de carbono diferentes, dando lugar a alcanos biciclicos. Este tipo de estructuras implican un carbono terciario o uno cuaternario, en uno de los átomos de carbono de la estructura cíclica. Es relevante remarcar esto ya que en el caso de los alcanos lineales y ramificados también se puede dar, pero no está implicito en la estructura; además este hecho conlleva bastantes propiedades químicas y físicas sobre la molécula en cuestión.

Alquenos
[editar]Los alquenos son compuestos similares a los alcanos pero en los cuales, dentro de la misma cadena de carbonos, un par de ellos (como mínimo) están unidos por un doble enlace, mediante una hibridación sp2. Al igual que en el caso de los alcanos este doble enlace le confiere unas propiedades características. Las cuales se comentarán en el apartado correspondiente a propiedades de los alquenos y demás.
Su fórmula general, al igual que en los cicloalcanos es:
Un ejemplo gráfico del tipo de enlace en estas moléculas es el que sigue:

Esa estructura se simplifica como:

donde son o hidrógeno o un radical tipo alcano (normalmente conocido como alquilo). Estos compuestos también tienen varios subtipos que implican diferentes propiedades. Estos subtipos se refieren a los compuestos con más de un doble enlace es decir pos alcapolienos, aquí pondremos como ejemplo tansolo alcadienos, es decir compuestos alquénicos con 2 dobles enlaces:
Los alcadienos, al tener dos dobles enlaces tienen 4 hidrógenos menos que un alcano, de modo que su fórmula general dejará de ser la de un alqueno, estos tendrán de fórmula general:
Alcadienos acumulados
[editar]
son aquellos en los que el mismo átomo de carbono posee dos dobles enlaces, uno a cada lado. Este átomo de carbono poseerá una hibridación sp dando un enlace lineal. Con uno de los orbitales p libre formará un enlace doble, o enlace , con uno de los átomos de carbono contiguos y con el otro orbital p libre, enlazará al otro átomo de carbono contiguo. Ambos átomos de carbono contiguos tendrán hibridación sp2, dando un enlace angular.
Alcadienos conjugados
[editar]
En este caso se observa que hay cuatro átomos de carbono con hibridación sp2 lo que quiere decir que hay 3 orbitales p libres contiguos y paralelos. Esto permite que los electrones se muevan por esos cuatro átomos dando una deslocalización que contribuye a la estabilidad de dichas moléculas. Es decir, como los electrones se pueden mover libremente, la molécula es más estable.
Este efecto se conoce como resonancia, y en el caso de los alquenos se puede ver claramente con el ejemplo del 1,3-pentadieno
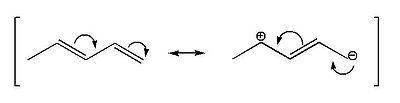
Alcadienos aislados
[editar]En este caso simplemente los dobles enlaces se encuentran separados por uno o más carbonos de tipo alcano, es decir con hibridación sp3, impidiendo toda resonancia y con lo cual haciendo que se comporten como dos alquenos totalmente independientes. tendran una orbita nebrutacionimica que lo hace que conserve su sustancia en buen estado y que los atomos logren separarse de la molecula.
Alquinos
[editar]Los alquinos, son similares a los alcanos, con la diferencia de que en estos dos átomos de carbono (como mínimo) están unidos por un triple enlace. Esto implica hibridación sp en los dos átomos de carbono, dando lugar a un enlace lineal. Un esquema de las interacciones entre orbitales es el siguiente:

Igual que con los alquenos, en los alquinos también puede haber alcapoliinos, pero cabe notar que en este caso jamás podrán ser acumulados ya que todos los orbitales están interaccionando ya con otros. Encambio si que pueden ser conjugados y aislados, siguiendo una relación igual que en la de los alcadienos. Por antonomasia en los triples enlaces conjugados también se producirá una resonancia entre los electrones

Un modelo tridimensional como ejemplo de un alquino sería el del 2-butino:

Alcoholes
[editar]Ahora cambia ya un poco el concepto de grupo funcional con respecto a los anteriores. En este caso las moléculas ya no están puramente constituidas de carbonos e hidrógenos. Sino que también habrá presentes cierta cantidad de átomos de oxígeno unidos por un simple enlace a un carbono y por un simple enlace a un hidrógeno. Es decir que son como alcanos en los cuales se ha sustituido un hidrógeno por un radical -OH (hidroxilo).
La fórmula general de los alcoholes es: donde x es un número entero entre 0 y 2n+2
un alcohol muy conocido es el etanol (alcohol etílico) que lo llevan las bebidas alcoholicas. Corresponde a la fórmula general donde n=2 y x=1:
Su fórmula estructural es la siguiente:

En este tipo de compuestos ya hay que tener en cuenta varios factores a la hora de adentrarse en su reactividad, ya que influye tanto la posición como el átomo de oxígeno que al ser más electronegativo "se lleva" hacia el los electrones del carbono adyacente, pudiendo atraer otros cercanos por inducción. Como este apartado es sólo descriptivo no nos adentraremos mucho en el tema.
Monoalcoholes
[editar]Como su nombre indica son moléculas en las que existe tan solo un átomo de oxigeno en forma de radical hidroxilo (-OH). Corresponden a una fórmula general: y presentan las propiedades típicas de un alcohol.


Polioles
[editar]Se trata de compuestos alcohólicos donde hay más de un átomo de oxígeno en forma de radical hidroxilo. y se corresponden con la formula general de los alcoholes. En esta sección, al igual que en la de los dobles enlaces (dienos, véase enlace Alcadienos acumulados) Pueden darse varios casos dependiendo de la posición respectiva de los alcoholes en la cadena carbonada. Como la variedad de estos casos es prácticamente nos pararemos en los dioles (x=2):
Dioles geminales
[editar]Son dioles en los cuales los dos radicales hidroxilo se encuentran en el mismo átomo de carbono:

Como se puede intuir, el tener dos grupos hidroxilo unidos al mismo átomo de carbono, se produce una gran deficiencia de electrones en este átomo por la menor electronegatividad de estos, esto será importante a la hora de entender la reactividad de este tipo de dioles.
Dioles vecinales
[editar]Son dioles en los cuales los dos radicales hidroxilo están unidos a dos átomos de carbono adyacentes (vecinales)

En este caso también se produce el mismo efecto que en el caso anterior tansolo que en este caso se produce una gran deficiencia electrónica en dos átomos de carbono adyacentes lo que hace que se debilite el enlace C-C haciendo que una mulécula de este tipo sea más sencilla de romper, o a la inversa, más difícil de obtener.
Dioles aislados
[editar]Al igual que en los dienos aislados los alcoholes aislados son aquellos en los que los grupos hidroxilo estan separados cuanto menos, por 1 carbono con hibridación sp3. Esto hará que (si no se producen efectos de inducción considerables) cada grupo hidroxilo tenga una reactividad independiente y se trate como si fueran dos alcoholes diferentes.

Aldehidos y Cetonas
[editar]En estos también habrá presentes cierta cantidad de átomos de oxígeno unidos por un doble enlace a un carbono . Es decir que son como alquenos en los cuales se ha sustituido un hidrógeno por un radical =O (carbonilo).
La fórmula general de los aldehidos y cetonas es:
La diferencia entre un aldehido y una cetona es que en el aldehido el carbonilo está al final de la cadena formando y en una cetona está en cualquier otra parte formando
Su fórmula estructural del aldehido más simple es el metanal formaldehído y es la siguiente:

En el caso de las cetonas se nombran usando generalmente Usando como referencia el carbón donde se encuentra el carbonilo las dos partes de la cadena de menor a a mayor con las que se une el grupo carbonilo. Como la acetona también llamada dimetilcetona.
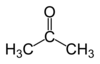
Ácidos carboxilicos
[editar]Como su nombre indica son moléculas en las que existe tanto un grupo con solo un átomo de oxigeno en forma de radical hidroxilo (-OH) y un grupo radical carbonilo (=O). Corresponden a una fórmula general: y presentan las propiedades típicas de un ácido. Generalmente estos se nombran poniendo la palabra ácido y luego el radical y la partícula oico. Existen muchos en la naturaleza pero el más común es el metanoico que se encuentra en el vinagre.

Aunque generalmente se les conoce con nombres más triviales en el caso de un curso de química se usarán las nomenclaturas IUPAQ.
Ácidos dicarboxilicos
[editar]Se trata de compuestos con dos grupos carboxilicos en ambos lados es decir que tienen ese grupo en ambos extremos estos también están presentes en la naturaleza.
Insaturados
[editar]También existen los ácidos carboxilicos insaturados y de estos derivan muchos ácidos grasos pero son igual su tratamiento que los hidrocarburos insaturados pero con la terminación de un ácido carboxilico al final de la cadena.
Amino
[editar]Ahora cambia de nuevo el concepto de grupo funcional con respecto a los anteriores. En este caso las moléculas ya también habrá presentes cierta cantidad de átomos de nitrogeno unidos por un simple enlace a uno o más carbonos y por uno o mas simples enlaces a un hidrógeno. Es decir que son como alcanos en los cuales se ha sustituido un hidrógeno por un radical (amino).
La clasificación general de las aminas es: Amina primaria Amina secundaria Amina terciaria
Estas cuando se combinan con oxígeno nos dan compuestos interesantes como son las amidas dentro de sus derivados tenemos los aminoácidos o la que más destaca que es la urea
Su fórmula estructural es la siguiente:



















